アプリケーション例
カーボンニュートラル関連分野として電池研究(リチウムイオン電池、イオン液体ゲル電解質)、二酸化炭素の分離回収、バイオサイエンス/ライフサイエンス関連分野(生体試料溶媒)での応用研究・アプリケーション例の一部を紹介しております。
イオン液体の概要や製品情報は以下からご覧ください。
カーボンニュートラル関連分野
近年地球温暖化や環境問題に対する意識が世界中で高まりつつあります。2015年に採択された「パリ協定」に基づき、世界各国で温室効果ガス削減に関する対策が実施されています。日本でも、2019年「パリ協定に基づく成長戦略としての長期戦略」を閣議決定し、“脱炭素化社会”実現を掲げました。そのような状況下でイオン液体は、ほかにはない特徴をもつ環境調和型材料としての利用に注目が集まっています。ここでは、エネルギー・電池研究分野でのイオン液体の利用、二酸化炭素の分離・吸収について紹介いたします。
エネルギー・電池研究分野
リチウムイオン電池
1991年にリチウムイオン電池が商品化されてから、現在も電気自動車の車載用途をはじめ、多くの媒体用に改良が続けられています。一般的なリチウムイオン電池は正極と負極の間に電解液が使われており、電解液の中をリチウムイオンが移動することで充電・放電をおこないます。
しかし、電解液には引火性の有機溶媒が使われることが多く、安全性の課題があります。イオン液体は、難揮発性・難燃性であり、高いイオン伝導性を示すことから電解液として利用することが検討・実現されてきました。1) 2)
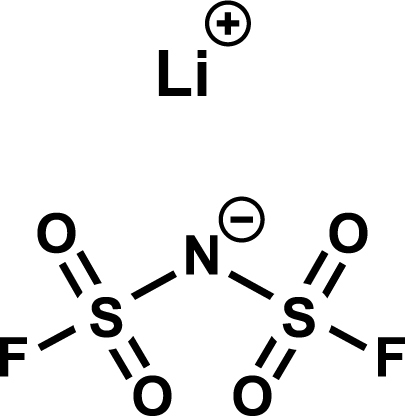
また、イオン液体には蒸気圧がほとんどなく、高真空下でも安定という特性があります。その特性を生かして宇宙環境を想定したリチウムイオン電池が開発されました。この電池にはLiFSA (LiFSI) (リチウム塩)とMPPyFSA(P13FSA) (イオン液体)が使われ、小型人工衛星「ほどよし衛星3号機」に搭載されました。2021年現在、「ほどよし3号」は地球周回軌道上にあり、イオン液体電池の作動に成功しています。この電池はラミネート外装で補強しただけで、宇宙空間という過酷な環境下にも耐えることができます。イオン液体電池は小型軽量化でき、高いバッテリー性能を有することが報告されました。3)
 |
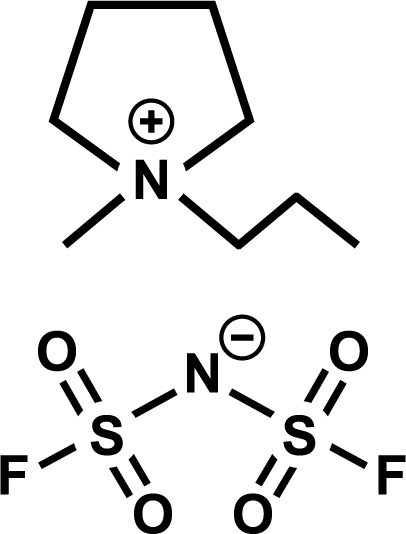 |
| LiFSA(LiFSI) | MPPyFSA(P13FSA) |
イオン液体ゲル電解質
イオン液体は、その特性から電解液として優れた性能を示しますが、液漏れなどの懸念が残されています。一方、イオン液体をゲル化した「イオン液体ゲル電解質」は安全性の高い、ゲル電解質として電気化学デバイスへの応用が期待され研究がおこなわれています。4)
ゲル化技術としては、重合による架橋ポリマー形成、ポリマーとの混合、低分子ゲル化剤、固体微粒子との混合など様々な方法が検討されてきました。しかし、ゲル化後にイオン伝導性が著しく低下するなどの課題もありました。5)6) これらの課題は新規ゲル化技術の開発により改善され、イオン液体と同等のイオン伝導性を維持できることが報告されています。7) 8) また、近年報告されたゲル化剤を使用すると0.1~2.0wt %という低い濃度でもゲル化、イオン伝導性が維持されることが報告されています。9)
二酸化炭素の分離・回収
イオン液体は窒素や水素などのガスをほとんど吸収しないが、二酸化炭素 (CO2)などの酸性ガスを選択的に吸収するという特性があり、二酸化炭素の分離・回収プロセスに利用可能なガス吸収液として知られています。アニオンにフッ素やトリフルオロメチル(CF3)基をもつイオン液体は、高いCO2の溶解度を示します。イオン液体のガス溶解度はカチオンよりもアニオンの依存性が高く、CO2との相互作用のため高い溶解度を示すことが報告されています。10) 11) 12)
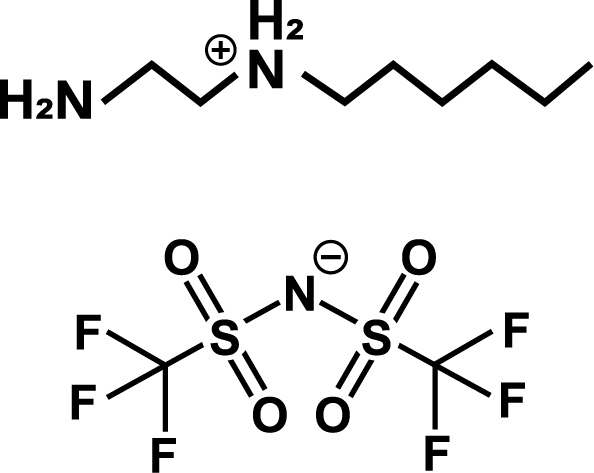
また、アミノ基 (NH2基) をもつイオン液体も同様にCO2の吸収が報告されています。アニオン部位にNH2基をもつ生体由来のアミノ酸系イオン液体は反応性が高く、優れたCO2吸収量を示し、幅広い温度域でCO2を吸収することが報告されています。13) 14) 高温でもCO2の吸収量が大きいことがわかっていますが、温度依存性が小さく、分離回収プロセスにおいてさらに高温条件が必要になるという欠点があります。カチオン部位に複数のNH2基をもつイオン液体は温度依存性が大きく、高温ではCO2を吸収しにくいため、加熱によりCO2が放散され、吸収液の再生が可能であることが報告されています。15)
 |
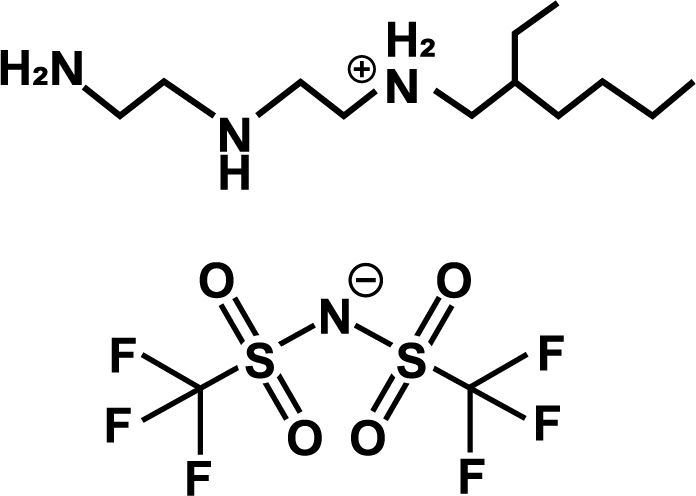 |
| [HexEDAH][TFSA] | [HexEDTAH][TFSA] |
現在、CO2の分離技術としてアミン溶液を利用したガス吸収法が利用されているが、CO2を回収するためには、ガス吸収後に加熱や減圧などの操作が必要となります。回収する際にアミン溶液は揮発しロスを生じるが、イオン液体は難揮発性であるため、この欠点をカバーできます。さらに、CO2の分離回収サイクルを複数回繰り返してもほとんど性能劣化しないという利点も報告されています。14)
加えて、CO2分離・回収に向けたイオン液体を含む分離膜の開発が進められています。CO2の分離膜法では分離操作において温度変化は必要とせず、連続的に高濃度のCO2を分離できるためプロセスの効率化が期待されます。イオン液体は難揮発性であるため分離膜中に保持され、高温高圧にも耐え、高い安定性を有しています。CO2/N2の選択性を付与することも可能であり、薄膜化技術が確立されれば実用化が期待されています。16) 17)
バイオサイエンス / ライフサイエンス分野
イオン液体は、合成溶媒、抽出溶媒、電気化学分野で必要不可欠な役割を果たす材料である一方、その独自の特性からバイオサイエンス / ライフサイエンス分野での用途が期待されています。
バイオリファイナリー / バイオマス溶解
バイオマスは地球上に多く存在する天然高分子で、再生可能な資源として注目されています。その応用は多岐にわたり、フィルム・繊維などの他にも、バイオエタノールの原料としても期待されています。バイオマスを実用化するにあたり、バイオマスを溶解し加工する必要があります。しかし、天然のバイオマスは分子内、分子間に強固な水素結合ネットワークを形成しており、一般的な溶媒に溶解することが困難でした。2002年にイオン液体によるセルロース溶解が報告されてから、バイオマス関連分野へのイオン液体の応用研究が活発に行われるようになりました。18)
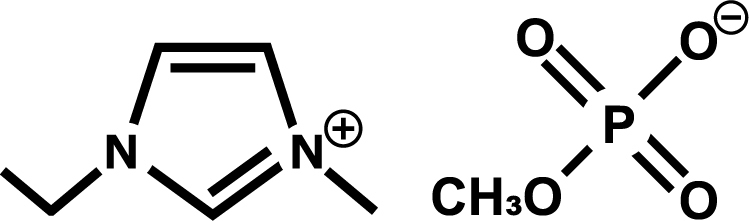
イオン液体の構造とセルロース溶解能が広く調査され、イミダゾリウムカチオンと亜リン酸アニオンからなる高極性イオン液体が非加熱条件下でセルロースを溶解させることが見出されています。19) 非加熱条件下でもセルロースが溶解されることが見出されましたが、少量の水が含まれると溶解能が失われてしまうことがわかっていました。そのため、セルロースを溶解する前に乾燥処理が必要であり、溶解プロセスを乾燥した密閉空間で行う必要がありました。
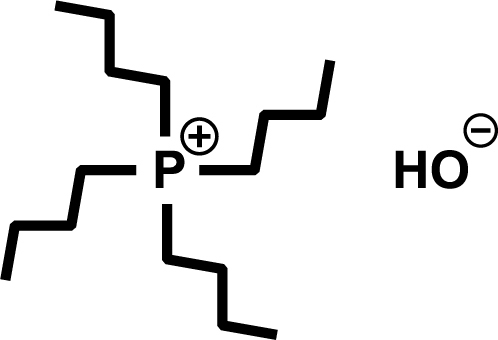
含水条件下でもセルロースを溶解するアルキルホスホニウムカチオンを有する水酸化物が見出され、多量の水を含んだ条件でのセルロース溶解が報告されています。20)
ライフサイエンス分野における新規溶媒としてのイオン液体
ライフサイエンス分野では、生体試料を凍結保存する場合や水に溶けない薬剤を溶解する場合に有機溶媒を使用することがあります。ライフサイエンス分野で使用される有機溶媒としてDMSO (ジメチルスルホキシド)が挙げられます。また、DMSOは細胞を保存するための凍結保護剤として働くことから古くから使用されてきました。しかし、DMSOの毒性は有機溶媒の中では比較的低いとされていますが、その毒性は完全に無視できるものではありません。DMSOは細胞透過性があり、細胞に様々な影響を及ぼすことが知られています。
カチオンとアニオンの両方を同一分子内に持つイオン液体である双性イオン液体は、生体試料を保存する新規の非水溶媒として期待されます。ヒスチジンに類似した構造をもつカルボン酸系双性イオン液体は常温で液体として存在し、水やDMSOへの溶解度が非常に低いセルロースなどを溶解し、非水溶媒としての可能性を示します。また、DMSO同様に凍結防止剤や疎水性薬物の溶媒として機能することがわかっています。
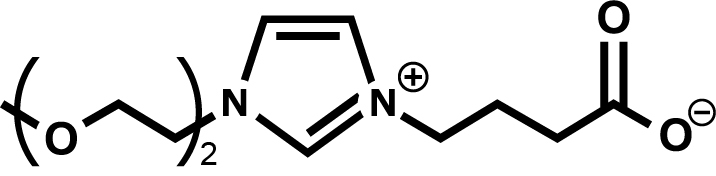
さらに、細胞生存率と細胞挙動の観点から、双性イオン液体がDMSOよりも低い毒性を示すことが報告されています。双性イオン液体はDMSO不溶性薬物を含む疎水性薬物を溶解し、双性イオン液体を含む凍結培地が、動物細胞を高効率で凍結保存することが確認されています。これらの結果は、双性イオン液体がライフサイエンスにおけるDMSOの代替溶媒として使用できる可能性が示されました。21)
参考文献
1) Sakaebe, H., Matsumoto, H., Electrochemistry Communications, 2003, 5, 594-598.
2) Watanabe, M., Thomas, L. M., Zhang, S.,Ueno, K., Yasuda, T., Dokko, K., Chemical Review, 2017, 117, 10, 7190–7239.
3) Yamagata, M., Tanaka, K., Tsuruda, Y., Sone, Y., Fukuda, S., Nakasuka, S., Kono, M., Ishikawa, M., Electrochemistry, 2015, 83, 918.
4) Karuppasamy K., Theerthagiri J., Vikraman D., Yim C.J., Hussain S., Sharma R., Maiyalagan T., Qin J., Kim H.S., Polymers.2020, 12, 918.
5) Noda, A.; Watanabe, M. Electrochim. Acta., 2000, 45, 1265.
6) Fuller, J.; Breda, A. C.; Carlin, R. T. J. Electrochem. Soc., 1997, 144, L67
7) Fujii, K.; Asai, H.; Ueki, T.; Sakai, T.; Imaizumi, S.; Chung, U.; Watanabe, M.; Shibayama, M. Soft Matter, 2012, 8, 1756
8) Nagasawa, J., Matsumoto. H., Yoshida. M., ACS Macro Lett., 2012, 1, 1108
9) Minakuchi, N., Hoe, K., Yamaki, D., Ten-no, S., Nakashima, K., Goto, M., Mizuhata, M., Maruyama, T., Langmuir, 2012, 28, 9259.
10) Aki, S. N.V.K., Mellein, B. R., Saurer, E. M., Brennecke, J. F., J. Phys. Chem.B, 2004, 108, 20355
11) Kazarian, S. G., Briscoe, B.J., Welton, T., Chem. Commun., 2000, 2047.
12) Seki, T., Grunwaldt, J.-D., Baiker, A., J. Phys. Chem. B., 2009, 113, 114.
13) Goodrich, B. F., de la Fuente, J. C., Gurkan, B. E., Lopez, Z. K., Price, E. A., Huang, Y., Brennecke, J. F., J. Phys. Chem. B., 2011, 115, 9140.
14) Makino, T., Kanakubo, M., Kamio, E., Takaba, H., Matsuyama, H., Fluid Phase Equilib., 2016, 420, 89.
15) 牧野貴至, 河野雅樹, 金久保光央, 熱測定, 2017, 44, 85.
16) Kasahara, S., Kamio, E., Yoshizumi, A., Matsuyama, H., Chem. Commun., 2014, 50, 2996.
17) Moghadam, F., Kamio, E., Yoshizumi, A., Matsuyama, H. Chem. Commun., 2015, 51, 13658.
18) Swatloski, R. P., Spear, S. K., Holbrey, J. D., Rogers, R. D., J. Am. Chem. Soc., 2002, 124, 4974.
19) Fukaya, Y., Hayashi, K., Wada, M., Ohno, H., Green Chem., 2008,10, 44.
20) Abe, M., Fukaya, Y., Ohno, H., Chem. Commun., 2012, 48, 1808
21) Kuroda, K., Komori, T., Ishibashi, K., Uto, T., Kobayashi, I., Kadokawa, R., Kato, Y., Ninomiya, K., Takahashi, K., Hirata, E., Commun. Chem., 2020, 3, 163.
無機試薬・素材研究に関する
お問い合わせ
メールでのお問い合わせ
お電話でのお問い合わせ
